Ngày 11/9 (giờ địa phương), Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) đã quyết định tạm hoãn kế hoạch tiêm chủng cho trẻ em dưới 5 tuổi để xem xét thêm dữ liệu về tính an toàn và hiệu quả của vaccine ngừa COVID-19 Pfizer với nhóm trẻ này.
Theo quyết định này, khoảng 18 triệu trẻ em dưới 5 tuổi ở Mỹ có thể sẽ phải đợi ít nhất đến tháng 4 để được tiêm chủng. Hiện nay, chính quyền Tổng thống Mỹ Joe Biden đang kỳ vọng có thể tiến hành tiêm vaccine cho trẻ từ 6 tháng tuổi đén 4 tuổi sớm nhất vào tuần tới bởi đây là nhóm duy nhất chưa được tiêm chủng tại nước này.
New York Times cho biết hãng dược Pfizer cùng công ty đối tac BioNTech đã đề nghị tạm hoãn tiêm sau khi họ phát hiện làn sóng biến thể Omicron đã dẫn đến tỷ lệ lây nhiễm cao hơn nhiều so với những gì họ ghi nhận trước đây ở các tình nguyện viên nhí trong thử nghiệm lâm sàng. Trong đó, dữ liệu mới cho thấy biến thể Omicron có khả năng né tránh vaccine tốt hơn so với biến thể Delta và hiệu quả của 2 liều vaccine hiện nay là không đủ.
Do đó, cả phía công ty và FDA đều thống nhất sẽ đợi thêm kết quả thử nghiệm mũi vaccine thứ 3, sẽ có kết quả vào tháng 4 tới.
Lượng kháng thể ở trẻ nhỏ còn thấp
Dữ liệu được công bố hôm 11/2 cho thấy rằng các mũi tiêm nhắc lại của vaccine Pfizer và Moderna sẽ mất đi một số hiệu quả đối với việc phòng nguy cơ cấp cứu và nhập viện sau khi tiêm 4 tháng. Cơ quan này nhận xét đây là một số bằng chứng sớm nhất về độ bền của mũi tăng cường. Trong khi các dữ liệu chỉ ra mũi tiêm thứ 3 cung cấp khả năng bảo vệ tốt hơn so với mũi tiêm thứ 2 nhưng câu hỏi đặt ra là khả năng bảo vệ đó kéo dài bao lâu.
Theo đó, 2 diễn biến hiện đã làm giảm bớt sự lạc quan về vaccine ngừa COVID-19 đồng thời cũng khiến chiến dịch tiêm chủng của Tổng thống Joe Biden phải tạm thời lùi một bước.
Các nhà nghiên cứu hy vọng vào tháng 4 tới, Pfizer và BioNTech sẽ có thể chứng minh rằng 3 mũi vaccine có khả năng bảo vệ trẻ em, với dữ liệu cho thấy phản ứng miễn dịch mạnh hơn và thành công hơn trong việc ngăn ngừa các triệu chứng bệnh.
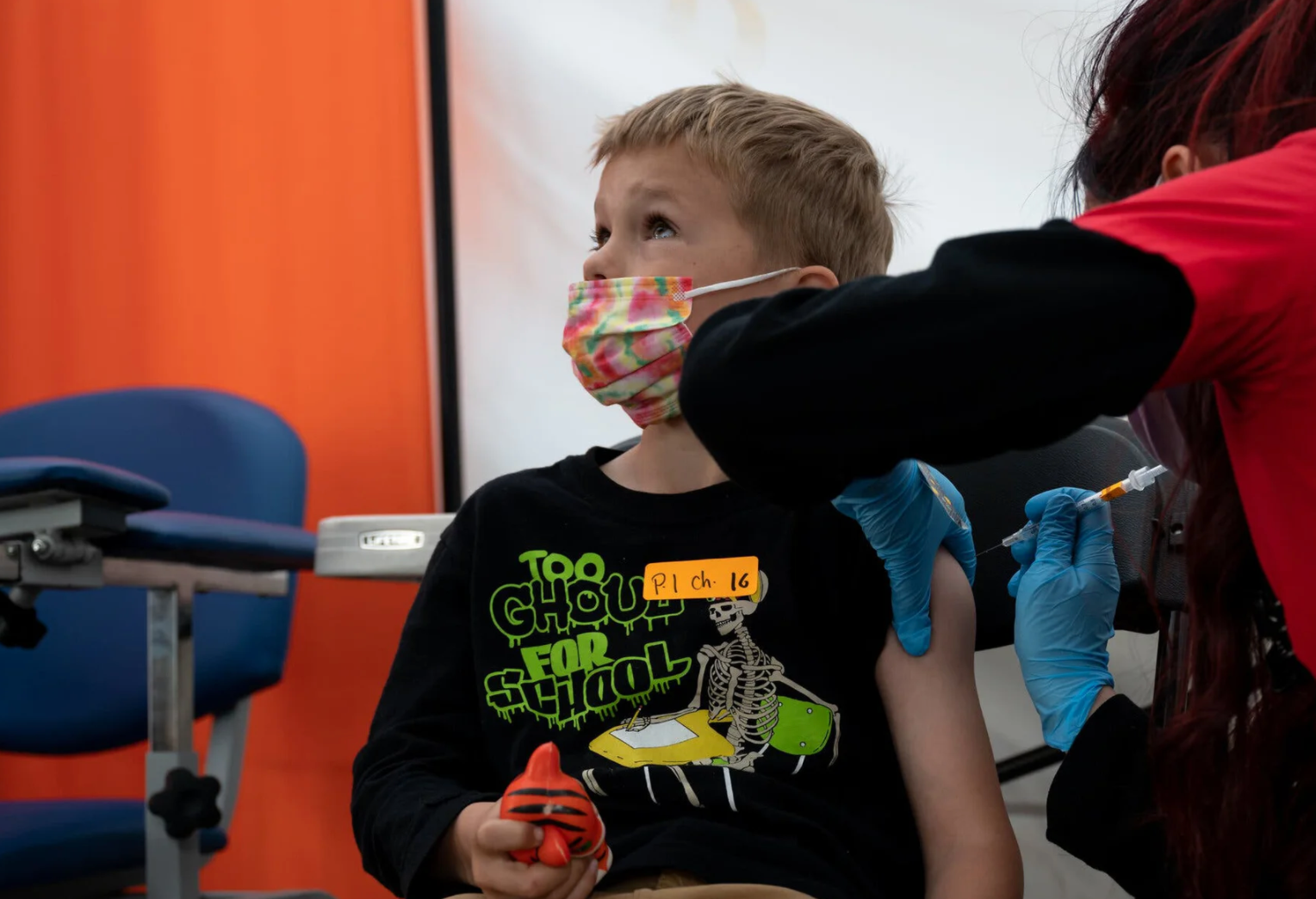
Các công ty cho biết trong một thông cáo báo chí rằng họ sẽ chờ dữ liệu về mũi tiêm thứ 3 với tốc độ nhanh chóng của nghiên cứu và vì họ "tiếp tục tin rằng nó có thể cung cấp mức độ bảo vệ cao hơn ở nhóm tuổi này".
FDA đã bắt đầu thúc ép Pfizer-BioNTech xin cấp phép cho phác đồ tiêm hai mũi cách đây vài tuần, bất chấp kết quả đáng thất vọng từ cuộc thử nghiệm được công bố vào tháng 12. Trẻ em từ 2 đến 4 tuổi chỉ tạo ra 60% lượng kháng thể mà thiếu niên và thanh niên đạt được. Nhóm tuổi lớn hơn được sử dụng làm tiêu chuẩn vì vaccine đã được chứng minh là có hiệu quả đối với họ.
Dù vậy, trẻ em từ 6 tháng tuổi đến 2 tuổi có thể tạo ra mức kháng thể được mong đợi. Các quan chức chỉ ra liều lượng vaccine tiêm cho nhóm này chỉ bằng 1/10 liều dùng cho những trẻ từ 12 tuổi trở lên và không gây lo ngại nghiêm trọng về an toàn.
Trong tháng này, Pfizer-BioNTech đã gửi yêu cầu cấp phép khẩn cấp và FDA đã lên lịch một cuộc họp của ủy ban cố vấn bên ngoài của họ vào thứ ngày 15/2. Cơ quan hy vọng sẽ có được sự khởi đầu từ việc tiêm phòng 2 mũi cho trẻ nhỏ và có khả năng tăng cường thêm một mũi thứ ba sau đó.
Tuy nhiên, vào cuối ngày 10/2, Pfizer đã cảnh báo FDA rằng họ đã có thêm dữ liệu gần đây, từ giữa tháng 1 trở đi, cho thấy một bức tranh đáng lo ngại hơn khi biến thể Omicron. Dữ liệu mới chỉ ra hai liều vaccine không đủ hiệu quả trong việc ngăn ngừa lây nhiễm bệnh có triệu chứng. Theo những người quen thuộc với nghiên cứu, căn bệnh này nhìn chung nhẹ và không có trẻ em nào phải nhập viện.
Trong một cuộc gọi với các phóng viên vào hôm 11/2, Tiến sĩ Peter Marks, quan chức hàng đầu của FDA là người ủng hộ chiến lược tiêm 2 mũi, cho biết dữ liệu mới nhất đã buộc họ phải tính toán lại. Ông chia sẻ: "Đúng, một số trong số những tính toán này đã bị phá vỡ nhưng đó là công việc của chúng tôi - điều chỉnh cho phù hợp với dữ liệu mới".
Nhiều chuyên gia nhi khoa đã thông cảm với nỗ lực ban đầu của FDA cân nhắc 2 liều vaccine cơ bản. Bên cạnh đó, một số người nhận định rằng các cơ quan quản lý đã đúng khi dừng lại.
Nhiều người lo ngại
Tiến sĩ James Conway, một chuyên gia về bệnh truyền nhiễm nhi khoa tại Đại học Wisconsin-Madison và một thành viên của Học viện Nhi khoa Mỹ, nhận xét: "Thành thật mà nói, tôi đã rất mừng khi lý trí và khoa học đã song hành và họ thực sự đã làm điều đúng đắn".
Tiến sĩ Conway cho biết ông lo ngại rằng việc cho phép một phần phác đồ vaccine cho trẻ nhỏ mà không có dữ liệu thuyết phục sẽ khiến người Mỹ gia tăng nghi ngờ rằng chính phủ liên bang đã cắt giảm các biện pháp.
Norman W. Baylor, cựu giám đốc văn phòng vaccine của FDA, cho rằng cơ quan đã đưa ra quyết định "lật ngược" về một vấn đề rất tế nhị, có lẽ vì áp lực của dư luận. Ông lưu ý, có nhiều bậc cha mẹ đã nói: "Tôi không quan tâm, họ chỉ cần cho con tôi tiêm 2 liều và ngay cả khi liều lượng vaccine rất nhỏ và chúng sẽ không được bảo vệ đầy đủ".
Tiến sĩ Baylor và một số chuyên gia khác đã đặt câu hỏi liệu có nhà phát triển vaccine nào chưa tìm ra liều lượng hiệu quả cho trẻ nhỏ nhất hay mức độ bảo vệ lâu bền đối với chúng hay chưa. Trong đó, Moderna hiện đang thử nghiệm liều lượng vaccine cao hơn so với vaccine Pfizer với trẻ em dưới 5 tuổi. Nhưng cho đến nay, vaccine của Moderna chỉ mới được phép sử dụng cho người lớn.
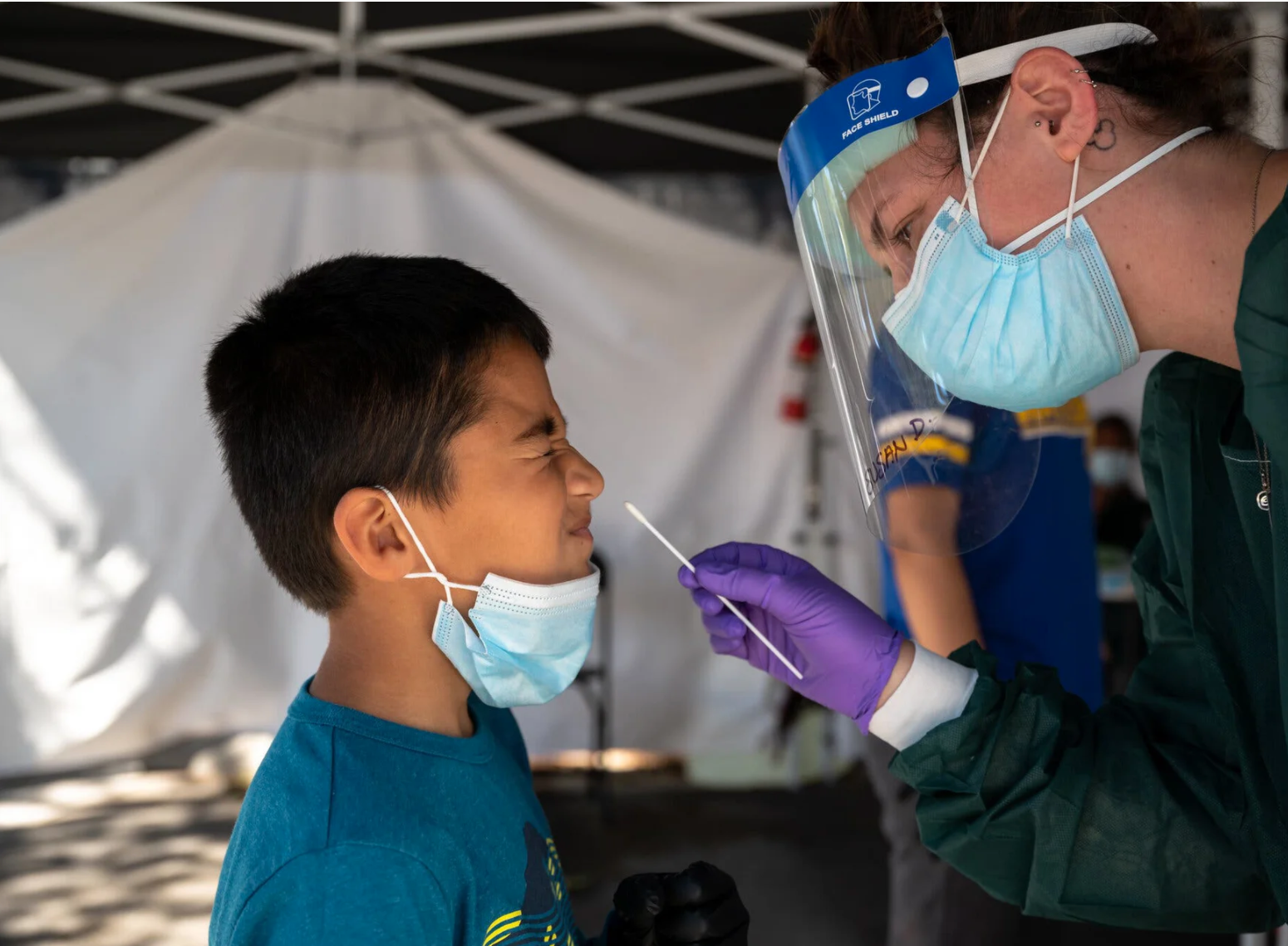
Các quyết định về vaccine gần đây của FDA đã rất khó khăn. Các quan chức y tế hàng đầu của chính quyền Biden đã thúc đẩy việc cấp phép cho các mũi tiêm nhắc lại vào mùa thu nhưng cuối cùng lại buộc phải giảm quy mô kế hoạch tiêm chủng của họ. Nhưng họ đã được minh oan khi biến thể Omicron cho thấy nó có thể dễ dàng né tránh 2 liều vaccine hơn so với biến thể Delta.
Đây không phải là lần đầu tiên FDA trì hoãn tiêm vaccine cho nhóm trẻ này. Ban đầu, Pfizer dự kiến công bố kết quả thử nghiệm vaccine với trẻ dưới 5 tuổi vào cuối tháng 12/2021. Tuy nhiên, kết quả cho thấy 2 mũi vaccine chỉ an toàn và mang tới khả năng bảo vệ cho trẻ sơ sinh dưới 6 tháng tuổi. Với trẻ từ 2 đến 4 tuổi, hai mũi vaccine không đủ tạo ra phản ứng miễn dịch đáng kể, khiến nghiên cứu phải bổ sung thêm mũi thứ 3.
Malia Jones, một nhà khoa học tại Đại học Wisconsin-Madison, người nghiên cứu tình trạng do dự tiêm vaccine ở trẻ em, dự đoán rằng các bậc cha mẹ thậm chí sẽ ít cho trẻ nhỏ tiêm chủng.Theo bà Jones, cha mẹ của những đứa trẻ trong độ tuổi này từ lâu đã có xu hướng tin những thông tin sai lệch về vaccine, bao gồm cả giả thuyết rằng chúng chứa đầy chất độc hoặc gây ra chứng tự kỷ.
Bà chia sẻ: "Theo dự đoán của tôi, tỷ lệ tiêm vaccine cho trẻ sẽ rất thấp".
Minh Hạnh (Theo NY Times)









