Tờ Tiền phong đưa tin, ông Nguyễn Minh Lợi, Vụ trưởng vụ Trang thiết bị và Công trình y tế (bộ Y tế), ngày 23/2 cho biết, bộ đã nắm được thông tin hiện nay có tình trạng khan hiếm cục bộ và giá cả không thống nhất đối với kit test SARS-CoV-2.
Để kịp thời có những biện pháp phù hợp, sáng cùng, bộ Y tế đã tổ chức cuộc họp trực tuyến với các doanh nghiệp sản xuất và nhập khẩu kit test SARS-CoV-2.
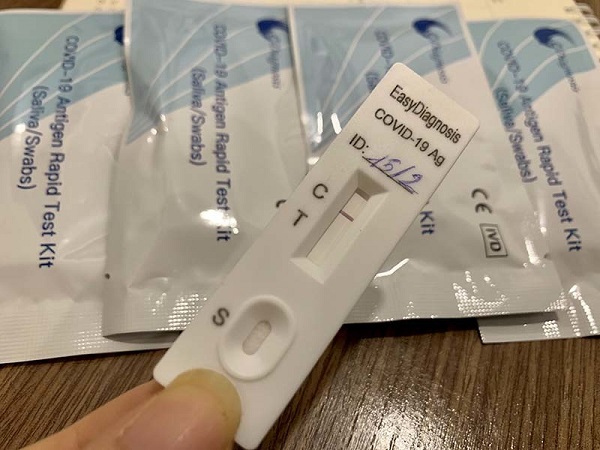
Theo Tri thức trực tuyến, bộ Y tế đã đưa ra 4 giải pháp nhằm kiểm soát giá kit test SARS-CoV-2.
Thứ nhất, bộ Y tế đề nghị các đơn vị sản xuất, nhập khẩu kit test SARS-CoV-2 chủ động tăng cường sản xuất, nhập khẩu sản phẩm để đảm bảo nguồn cung trên nguyên tắc đảm bảo chất lượng sản phẩm.
Các doanh nghiệp có trách nhiệm công khai và cập nhật giá. Các nhà phân phối, bán lẻ thực hiện niêm yết giá, không gom hàng và tăng giá; không để tình trạng giá công bố cao nhưng giá bán thấp, tạo kẽ hở cho các nhà phân phối, bán lẻ lợi dụng làm lũng đoạn thị trường; không bán cho các đơn vị thu mua, đầu cơ để tăng giá khi nhu cầu trong nước đang tăng cao, gây khan hiếm thị trường.
Thứ hai, bộ Y tế có các hướng dẫn cụ thể đối với những trường hợp nguy cơ (F1) và F0. Các quy định này đều được công khai.
Vì vậy, ông Lợi đề nghị người dân nghiên cứu, liên hệ với các cơ sở y tế gần nhất để được hướng dẫn chi tiết, tránh việc mua và sử dụng kit xét nghiệm khi chưa có nhu cầu, gây lãng phí không cần thiết, ảnh hưởng đến thị trường.
Trường hợp cần thiết, người dân lưu ý khi mua và sử dụng các sản phẩm lưu hành trên thị trường phải có nguồn gốc rõ ràng. Điều kiện bắt buộc là những kit test phải nằm trong danh sách sản phẩm đã được bộ Y tế cấp phép lưu hành và giấy phép nhập khẩu theo đúng thông tin về chủng loại, hãng nước sản xuất, nhãn mác đầy đủ thông tin theo quy định và có tài liệu hướng dẫn sử dụng bằng tiếng Việt.
Bộ Y tế khuyến cáo người sử dụng nghiên cứu kỹ và thực hiện theo đúng hướng dẫn sử dụng sản phẩm để tránh mua phải hàng giả, không rõ nguồn gốc xuất xứ, kém chất lượng
Thứ ba, bộ Y tế đã gửi văn bản tới UBND các tỉnh, thành phố về việc phối hợp chỉ chủ động hoạt động sản xuất, kinh doanh khả năng cung ứng trang thiết bị y tế phòng, chống dịch COVID-19 và đảm bảo bình ổn giá trang thiết bị y tế.
Thứ tư, bộ Y tế sẽ phối hợp với cơ quan quản lý giá, quản lý thị trường, hải quan và các đơn vị liên quan thực hiện việc thanh tra, kiểm tra một số đơn vị về việc kê khai và công khai giá bán theo quy định, đảm bảo giá bán ra phù hợp với với các chi phí đầu vào, không bán qua nhiều cấp trung gian, tăng giá bất hợp lý để đảm bảo bình ổn giá bán trên thị trường.
Thống kê của bộ Y tế cho thấy, tính đến ngày 23/2, bộ đã cấp phép 169 trang thiết bị y tế, sinh phẩm chẩn đoán in vitro xét nghiệm SARS-CoV-2, có 14 sản phẩm sản xuất trong nước và 155 sản phẩm nhập khẩu (gồm 56 sản phẩm xét nghiệm vật liệu di truyền, 83 sản phẩm xét nghiệm kháng nguyên SARS-CoV-2 và 30 sản phẩm xét nghiệm kháng thể kháng SARS-CoV-2).
Các trang thiết bị y tế, sinh phẩm chẩn đoán in vitro xét nghiệm SARS-CoV-2 là các trang thiết bị y tế loại C, D nên khi lưu hành trên thị trường phải được cấp số lưu hành hoặc giấy phép nhập khẩu theo quy định.
Các cơ sở kinh doanh loại sản phẩm này phải công bố đủ điều kiện mua bán trang thiết bị tế loại C, D theo quy định của Nghị định số 98/2021/NĐ-CP ngày 8/11/2021 của Chính phủ về quản lý trang thiết bị y tế.
Hoa Vũ (T/h)









